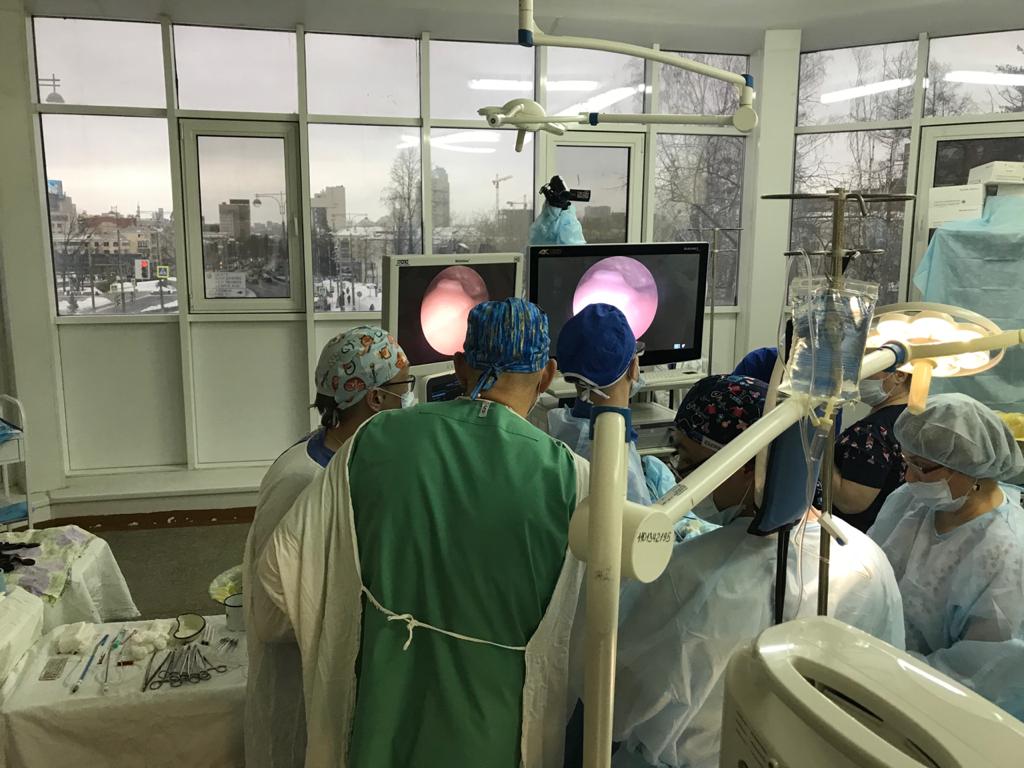
Внутриутробная хирургия в НИИ ОММ
- Категория: Материалы для пациентов
- Просмотров: 46397
|
Зав. ОБФЛ ФГБУ «НИИ ОММ» МЗ РФ, д.м.н., врач УЗД высшей категории Косовцова Н.В. |
К.м.н., врач акушер-гинеколог высшей категории Маркова Т.В. |
|
Заочный аспирант, врач УЗД, врач УЗД Поспелова Я.Ю. |
К.м.н., врач акушер-гинеколог высшей категории Осипова Л.Е. |
Появление и быстрые темпы развития фетальной хирургии стало возможным благодаря современным системам визуализации в режиме онлайн, совершенствованию инструментария и оборудования, позволяющего без последствий проникнуть в особый мир внутриутробного развития. К сожалению отечественной аппаратуры для фетальных операций не разработано.
Необходимость рассмотрения в некоторых случаях плода как пациента связана с возможностью коррекции ранее тяжелых патологических состояний, включающие некоторые аномалии развития, фето-фетальной трансфузионный синдром близнецов, тяжелые формы гемолитической болезни плода. Спектр патологий плода подлежащих внутриутробной коррекции с каждым годом расширяется, разрабатываются и совершенствуются новые технологии. Сегодня в практику института внедрено более 10 фетальных методик, что требует импортных расходных материалах, которые в настоящее время Россией не закупаются. Мы готовы участвовать в разработке инструментария с нашими отечественными производителями, но для этого требуются немалые средства.
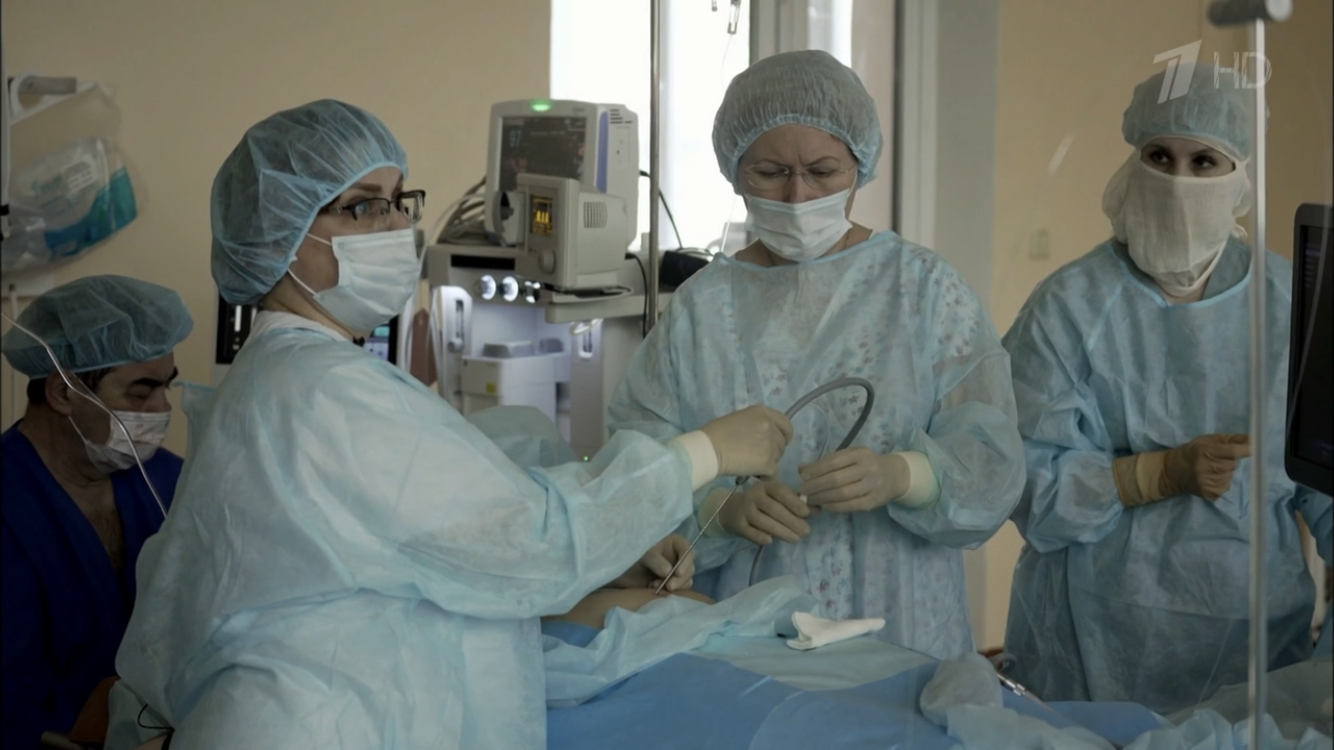
Внутриутробная хирургия объединяет врачей различных специальностей – акушеров-гинекологов, неонатальных хирургов, анестезиологов-реаниматологов, специалистов биофизической и лучевой диагностики, трансфузиологов. В настоящее время в НИИ ОММ проводятся внутриутробные операции совместно с детскими нейрохирургами, сосудистыми хирургами, урологами. Наши анестезиологи владеют методами обезболивания не только беременной женщины, но и плода.
Проблемами внутриутробной хирургии занимается Международное сообщество «Плод как пациент», - междисциплинарная группа врачей, которые работают над совершенствованием диагностики патологии и терапии плода. Российская Федерация не исключение. В ноябре 2017 года, в С-Петербурге пройдет уже II съезд Российской ассоциации специалистов медицины плода. Молодых исследователей этой отрасли медицины стремится поддерживать общество фетальных хирургов (IFMSS). На многочисленных форумах и съездах подвергаются дискуссии не только профессиональные, но и этические проблемы.
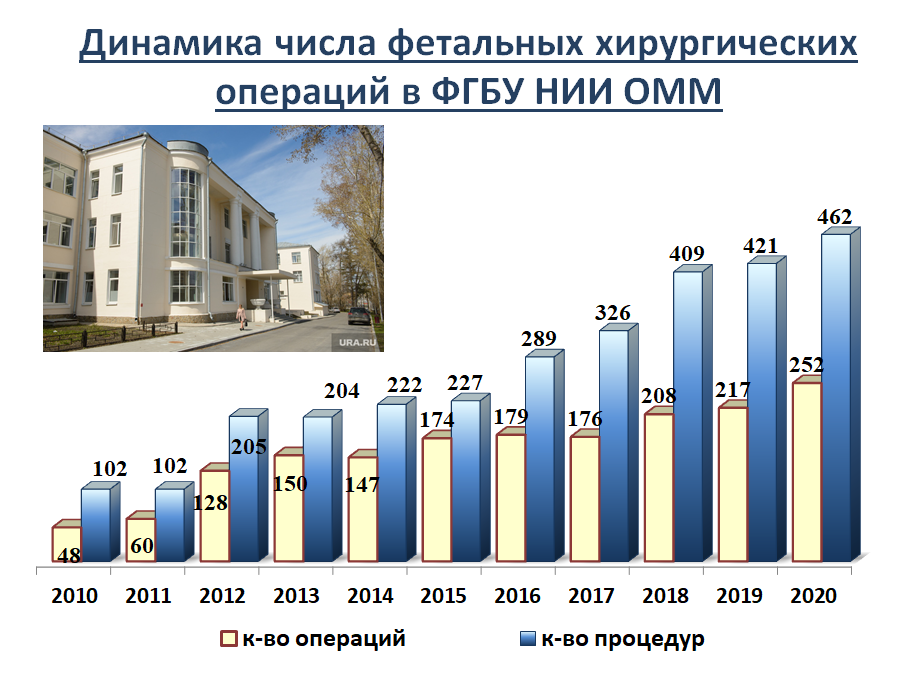
В ФГБУ НИИ «Охраны материнства и младенчества» (ФГБУ «НИИ ОММ») с апреля 2009 г начато внедрение методов фетальной хирургии. Опыт, накопленный с этого момента, позволяет нам в большинстве случаев не только точно диагностировать патологию плода, но и разрабатывать протоколы внутриутробных операций.
 На сегодняшний день институт ставит перед собой задачу освоения внутриутробной коррекции нейрохирургической патологии. В содружестве с Тюменским Федеральным нейрохирургическим центром в клиническую практику внедрена операция по внутриутробной коррекции гидроцефалии (рис 1,2).
На сегодняшний день институт ставит перед собой задачу освоения внутриутробной коррекции нейрохирургической патологии. В содружестве с Тюменским Федеральным нейрохирургическим центром в клиническую практику внедрена операция по внутриутробной коррекции гидроцефалии (рис 1,2).
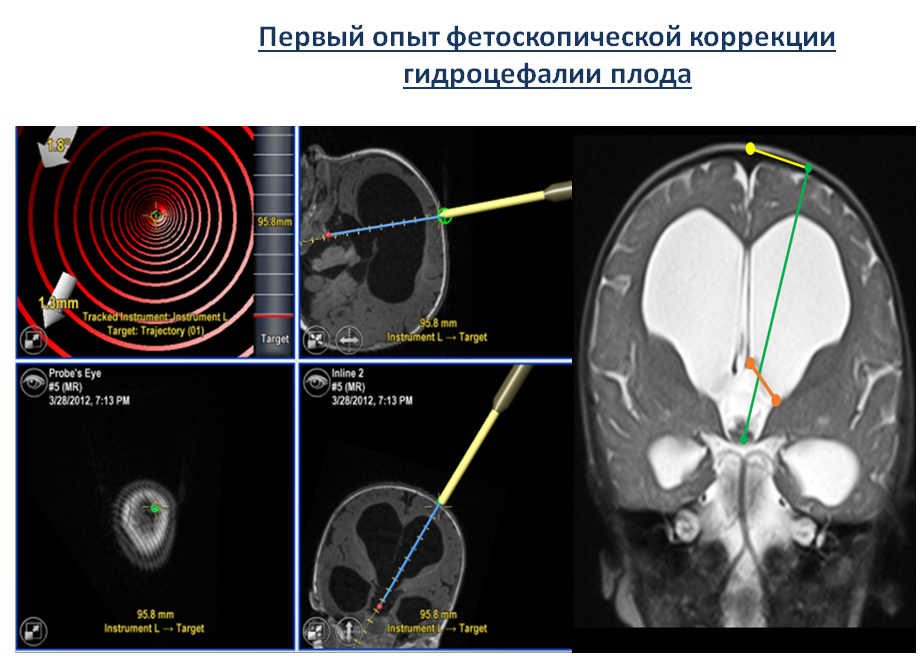
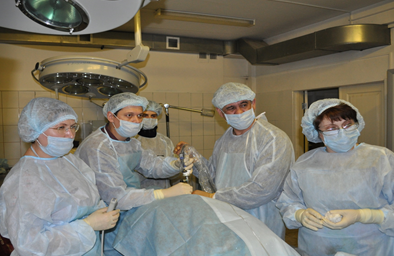 Рисунок 1. I этап эксперимента по внутриутробной коррекции гидроцефалии.
Рисунок 1. I этап эксперимента по внутриутробной коррекции гидроцефалии.
Рисунок 2. В операционной. Врачи:д.м.н., профессор Косовцова Н.В, д.м.н.,, к.м.н Маркова Т.В., Фоминых Н.В.Операционная сестра –Рябкова Е.
За проведение первой в мире удачной вентрикулоцистерностомии у плода при тривентрикулярной гидроцефалии врачи (д.м.н., профессор Косовцова Н.В, д.м.н.,профессор Суфианов А.А.,к.м.н Якимов Ю.А.,к.м.н Маркова Т.В., Фоминых Н.В.) удостоены премии «ПРИЗВАНИЕ» (2021г), в номинации «УНИКАЛЬНАЯ ОПЕРАЦИЯ». (рис 3,4,5)
Рисунок 3.Награждение лауреатов премии «ПРИЗВАНИЕ» министром здравоохранения М.А. Мурашко.
Рисунок 4.Д.м.н., профессор Косовцова Н.В, д.м.н.,профессор Суфианов А.А.,к.м.н Якимов Ю.А.,к.м.н Маркова Т.В., Фоминых Н.В.2021г
Рисунок 5.Д.м.н., профессор Косовцова Н.В, д.м.н.,профессор Суфианов А.А.,к.м.н Якимов Ю.А. после вручения премии «ПРИЗВАНИЕ»
В статье представлен опыт по коррекции патологии плода методами внутриутробной хирургии сотрудников ФГБУ «НИИ Охраны материнства и младенчества» Минздрава России. Внутриутробные манипуляции проводимые в нашем институте прошли клиническую апробацию в экспериментах на животных и утверждены этическим комитетом.
Крестцово-копчиковая тератома (ККТ) – Крестцово-копчиковая тератома (ККТ) является наиболее распространенной опухолью, встречается примерно в 1 из 40 000 живорождений (Altman et al., 1974). ККТ представлены тремя видами зародышевых клеток (эктодермы, мезодермы и энтодермы), и эмбриологически происходят от узла Хенсена (Teilum, 1965). Большинство ККТ возникают спорадически, но были описаны несколько семей с аутосомно-доминантным типом наследования ККТ (Gopal et al., 2007). Ультразвуковая пренатальная диагностика позволила диагностировать ККТ еще в начале второго триместра. Плоды с небольшими ККТ не имеют перинатальных проблем. У плодов с большими ККТ перинатальная смертность связана с декомпенсацией сердечно-сосудистой системы, с артериовенозным шунтированием в пределах крупной сосудистой сети опухоли с развитием водянки плода (Bondet al., 1990). Несколько типов внутриутробного вмешательства были предложены у плодов с плохим прогнозом. Несмотря на то, что первая успешная открытая хирургическая резекция ККТ была выполнена в 1997 году (Adzick et al., 1997), открытая хирургия зачастую связана с угрозой преждевременных родов, хориоамнионита, внутриутробной гибелью плода и материнской заболеваемости (Bullard and Harrison, 1995; Langer et al., 1989). Были также предприняты попытки минимально-инвазивных методов, таких как радиочастотная абляция (RFA) или шунтирование кист опухоли (Adzick et al., 2003). Однако критерии для необходимости пренатальных вмешательств в ККТ остаются неясными. [1]
В нашей практике мы провели 4 случая чрескожного мини инвазивного лечения ККТ. Показания к оперативному лечению формировались при ультразвуковой и МРТ оценке состояния плода и опухоли.
При ультразвуковом исследовании мы определяли:
- Выраженность кистозного и эхогенного компонентов (>50%);
- Темп роста тератомы (быстрым считался рост опухоли 1 см и более в 2 недели;
- При Doppler исследовании определяли составляющие сосудистой сети опухоли.
- Регистрировались допплерометрические изменения кровотока в нижней полой вене, венозном протоке, вене пуповины, трикуспидальная регургитация
- Подтверждался экзофитный рост опухоли;
- Объем опухоли был рассчитан с использованием трехмерной ультразвуковой системы VOCAL;
- Наличие водянки плода
Для определения типа ККТ мы применяли МРТ и использовали классификацию Американской академии детской хирургии:
Тип I: развивается только за пределами плода (может иметь небольшую сакральную составляющую); встречается в большинстве случаев, 47%
Тип II: с внутритазовой и сакральной составляющей
Тип III: экстра эмбриональная составляющая с брюшно-тазовой локализацией
Тип IV: опухоль полностью развивается в тазу плода.
Показаниями к внутриутробному лечению послужили:
- быстрый рост опухоли,
- преимущественно экзофитный рост,
- преимущественно эхогенный компонент опухоли (>50%)
- TFR ( tumor volume-to-fetal weight ratio) был выше 0.12 cm3/g
- срок беременности до 28 нед
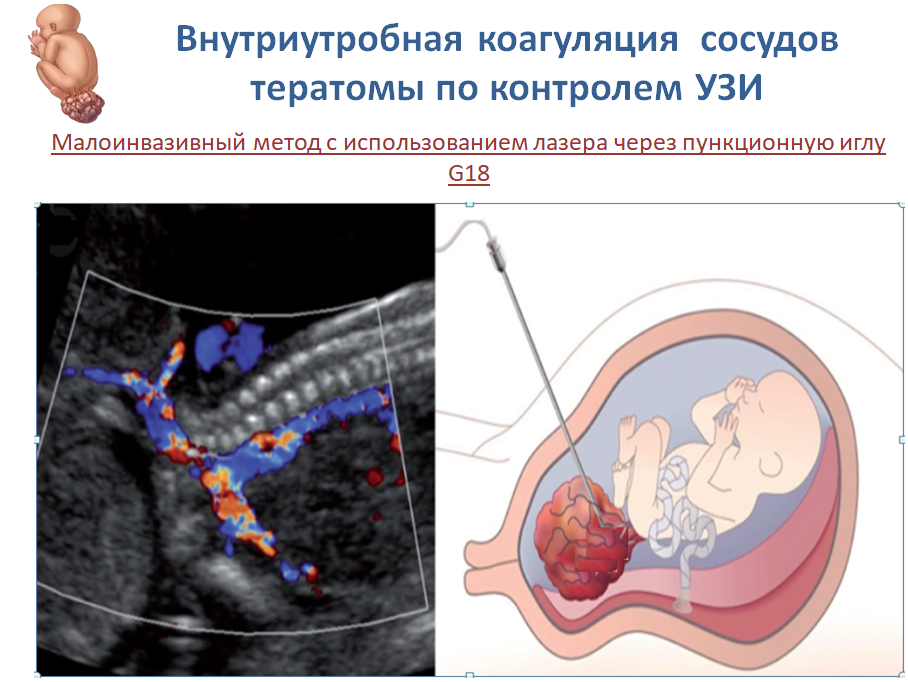
Для лечения ККТ мы применяли лазерную коагуляцию питающих ККТ артерий.
Операции по коагуляции сосудистой ножки ККТ проводились в сроке от 21 до 26 нед беременности. Средний срок проведения манипуляции 25,3 нед. Средний возраст пациенток 28,3 года. В 3 пациентка были первобеременные, 1 пациентка повторнобеременная, повторнородящая. Соматический и акушерский анамнез у пациенток был не отягощен. Все опухоли были I-II типа. Водянка у плода была зарегистрирована в 1 случае. Прооперировано 4 пациентки. Эффективность манипуляции составила 50%. В 1 случае коагуляции сосудистой ножки тератомы у плода с неиммунной водянкой произошли преждевременные роды в сроке беременности 28 нед. Во втором случае произошло увеличение внутри тазовой и сакральной составляющей опухоли, что вызвало появление двухстороннего гидронефроза у плода, было проведено прерывание беременности по желанию пациентки и медицинским показаниям. В 2 случаях пациентки были родоразрешены в доношенном сроке. Окончательное удаление опухоли проводилось после рождения плодов (рис. 6,7).
Рисунок 6. Схема внутриутробной лазерной коагуляции питающих сосудов тератомы.
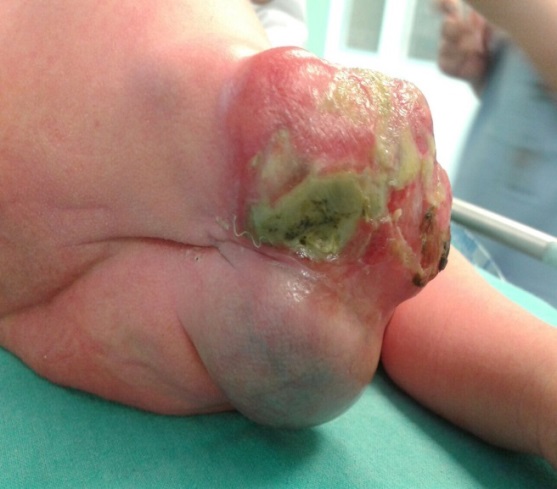
Рисунок 7. Крестцово-копчиковая тератома у новорожденного после коагуляции сосудистой ножки тератомы в 22 недели беременности
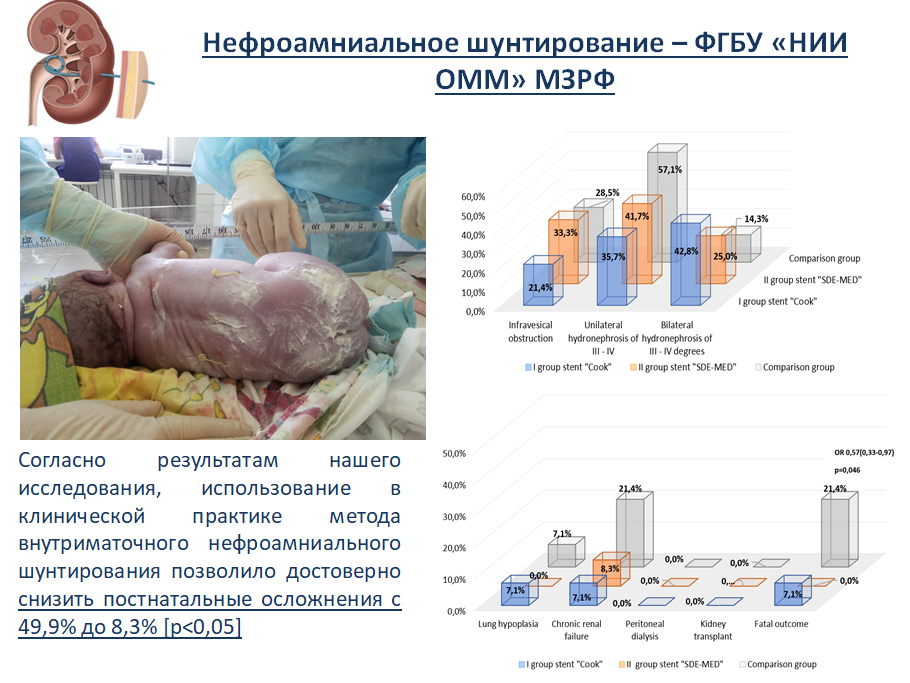
Обструкция мочевыводящих путей у плода. Благодаря современным методам инструментальной диагностики выявляется широкий спектр патологии мочевыводящей системы плода (от агенезии до транзиторной пиелоэктазии). Внутриутробные вмешательства в пренатальном периоде могут оказаться эффективными только при некоторых аномалиях [2, 3]. Наилучшие показатели выживаемости, на основании данных «Международного общества терапии и хирургии плода», регистрируются у плодов с диагнозом заднего уретрального клапана. [4, 5]. Нами проведено 27 шунтирующих операций почек плода при обструктивных поражениях мочевыделительного тракта у 19 пациентки с положительным эффектом. Показаниями для оперативной коррекции патологии мочевыводящих путей плода были: синдром задних уретральных клапанов, двухсторонние/односторонние гидронефрозы III-IV степени. Шунтирующие операции на мочевом пузыре нами применяются редко и на более поздних сроках беременности, т.к. почечная паренхима фиксирует стент лучше. Первое стентирование во всех случаях проводилось в сроке беременности 22-28 недель. Повторные шунтирования осуществлялись при ультразвуковых признаках выпадения стента из почки. Целью операции является создание оттока мочи из почки плода в амниотическую полость.
Рисунок 8. Стент в почке плода
Для шунтирования почек мы применяли неонатальные стенты-эндопротезы фирмы «Cook» 3 Fr, роль проводника для стента выполняла спинальная игла 16G (рис. 8).
С учетом практического опыта ФГБУ «НИИ ОММ» по шунтирующим операциям на мочевыделительном тракте плодов, разработан и изготовлен отечественный стент для внутриутробного нефро-амниального шунтирования (рис. 9). Наш стент имеет разнонаправленные спиральной формы пигтейлы и минимальный диаметр 3 Fr. Данное отечественное изделие апробировано в ряде экспериментов, запатентовано и в настоящее время проходит государственную регистрацию [6].
 Рисунок 8. Общий вид набора для шунтирующих операций при пороках развития мочевыделительной системы плода разработанный сотрудниками ФГБУ «НИИ ОММ».
Рисунок 8. Общий вид набора для шунтирующих операций при пороках развития мочевыделительной системы плода разработанный сотрудниками ФГБУ «НИИ ОММ».
В 2017 г за внедрение внутриутробного нефро-амниального шунтирования врачам д.м.н. профессору Косовцовой Н.В., д.м.н., профессору Башмаковой Н.В., к.м.н. Марковой Т.В. вручена премия «ПЕРВЫЕ ЛИЦА» (Рисунок 9).

Рисунок 9. Премия «ПЕРВЫЕ ЛИЦА».
3. Патология монохориальных двоен: Синдром межблизнецовой трансфузии (ФФТС – фето-фетальный трансфузионный синдром) формируется в 25-30% двоен. Основоположники внутриутробного лечения фето-фетального трансфузионного синдрома J.E.De Lia et al. (1999), R. Quintero (2002), J. Deprest (2002) с успехом применили лазерную коагуляцию плацентарных сосудов, а K.Benirschke et al. (1973) и B.K.Wittman et al. (1986) предлагали перевязку сосудов пуповины [7].
Основные методы коррекции которые применяются при синдроме трансфузии это: септотомия (часто сочетается с амниоредукцией), серия амниоредукций (частота выживаемости хотя бы одного плода 60-70%); неврологические нарушения 24%); лазерная коагуляция сосудистых анастомозов в плаценте (частота выживаемости 70-90%, неврологические нарушения 8%) [8,9,10].
В нашей клинической практике мы применяли все методики по коррекции ФФТС: серии амниоцентезов, септотомии, до селективной коагуляции плацентарных анастомозов, которая явилась наиболее эффективным методом лечения (рис. 10).С 2010 по 2020 год проведено 258 операции лазерной коагуляции плацентарных анастомозов. Коррекция ФФТС проводилась при наличии II-IV степени синдрома, эффективность лечения составила 89% для одного плода и 69% для двух плодов [11 - 13].
Как показывает практика, пациенты с ФФТС направляются в специализированные центры на более поздних стадиях. Запоздалая диагностика данного синдрома, особенно при ранней манифестации (до 20 недель), сопряжена с наименьшим процентом положительных перинатальных исходов. В настоящее время прогноз зависит от своевременной диагностики и метода лечения при отсутствии коррекции прогноз, как правило, неблагоприятный и связан с высокой долей перинатальных потерь 70-90%.
Особую актуальность приобретает поиск диагностических критериев позволяющих прогнозировать формирование ФФТС на доклиническом этапе. На базе ФГБУ «НИИ ОММ» проводится научное исследование которое направлено на изучение роли про и антиангиогенных факторов роста и полиморфизмов генов ассоциированных с нарушением ангиогенеза при патологиях монохориальной многоплодной беременности. Изменения ангиогенного статуса беременной на определенных этапах формирования плаценты, может быть одним из механизмов связывающими аномальную плацентацию с развитием фето-фетального трансфузионного синдрома. Фундаментальные исследования патогенеза ФФТС позволит в дальнейшем перейти на качественно новый уровень в области коррекции синдрома трансфузии и селективной задержки роста плода при монохориальном многоплодии.
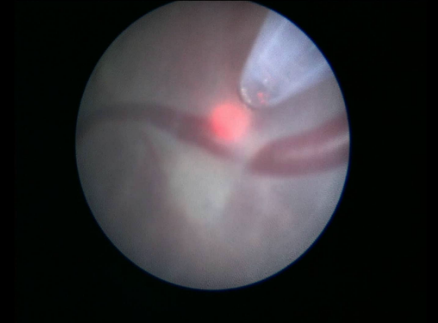
Рисунок 10. Лазерная коагуляция плацентарных анастомозов
4. Селективный фетоцид – применяется при дискордантных аномалиях, в частности, при монохориальном многоплодии, когда один из плодов представляет угрозу для другого или создает риск прерывания беременности. В этих случаях редукция одного плода улучшает шансы другого и предотвращает прерывание беременности.
Окклюзия сосудов пуповины, является одной из методик фетоцида, и впервые начала применяться в пренатальной медицине с 70-80 гг. прошлого столетия при осложненном течении монохориальной двойни.
Полное прекращение кровотока по сосудам пуповины обеспечивает их окклюзия и профилактирует острую кровопотерю у живого плода при гибели одного близнеца из монохориальной двойни, что приводит к его грубым неврологическим нарушениям вплоть до гибели. В период с 2010 по 2014 гг. был сформирован единый информационный массив, содержащий сведения о материнском акушерско-гинекологическом и соматическом анамнезе, особенностях течения настоящей беременности, способах родоразрешения, течении послеродового периода, перинатальных исходах монохориальных двоен. Из базы данных выделена группа из 40 пациенток, у которых была проведена лазерная коагуляция сосудов пуповины под контролем ультразвукового исследования [14].
На сегодняшний день мы испытываем большие трудности при обсуждении пациентов, которым необходимо применить операцию фетоцида, т.к. в Российском законодательстве не прописаны показания к проведению данной манипуляции. Нет протоколов и порядка ее проведения. Четко не обозначены пороки развития плода, при которых в любые сроки беременности возможно проведение фетоцида.
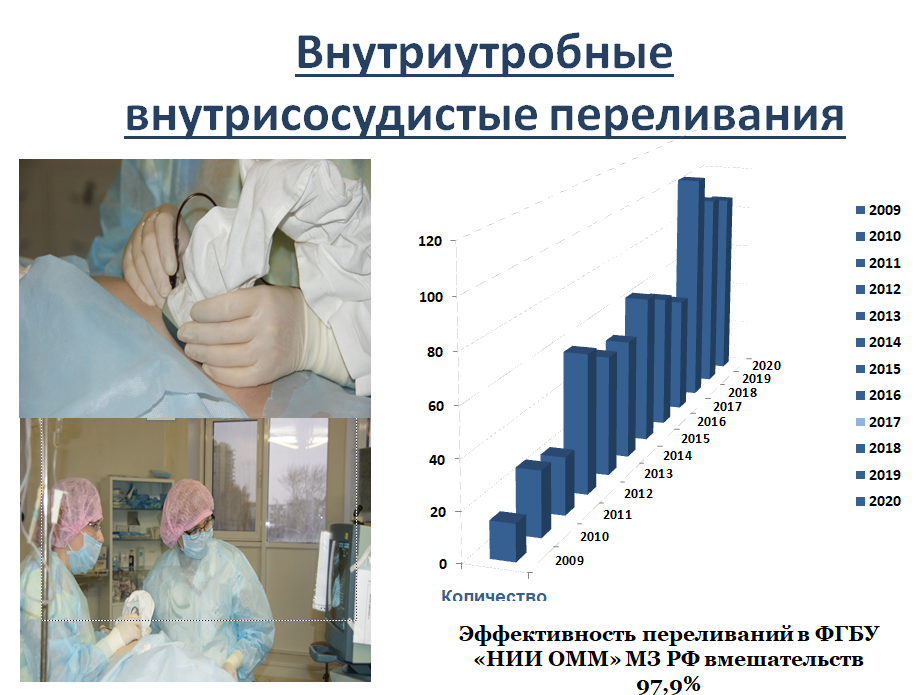
5. Внутриутробное, внутрисосудистое переливание крови проводится для внутриутробной коррекция анемии, в большинстве случаев вызванной резус-конфликтной беременностью. Впервые лечение гемолитической болезни плода применили в 1977 г., когда Cooperberg P.L. провел первую интраперитонеальную трансфузию под контролем ультразвука, а в 1981 г. Rodek C.H. – первую внутрисосудистую трансфузию [15]. В настоящее время в России технологией внутриутробных гемотрансфузий владеют 8 перинатальных центров. В случаях наличия ультразвуковых признаков анемии у плода проводится диагностический кордоцентез. В ситуации с уровнем Ht<30% и Hb<90 г/л необходимо проведения внутриутробной гемотрансфузии плоду. Единственным эффективным методом лечения гемолитической болезни плода является проведение внутриутробных внутрисосудистых гемотрансфузий. В ФГБУ «НИИ ОММ», начиная с 2009 г., проведено 385 внутриутробная внутрисосудистая гемотрансфузия у 161 женщины в сроках беременности от 19 до 33-34 недель. Средний срок родоразрешения – 33,3 недели. Эффективность лечения составила 97,3%. Дети растут и развиваются нормально (рис 11.).
Рисунок 11. Внутриутробное, внутрисосудистое переливание крови.
6. Операции при диафрагмальной грыже плода. Harrison MR et al. в 1998 г. впервые опубликовал свои положительные результаты фетоскопической трахеальной окклюзии на человеческих плодах с помощью интратрахеально заполняемого пеной развертывающегося баллона. Данный вид операций внедрен в нашей клинике [16 - 18]. На сегодняшний день проведено 6 операций баллонной окклюзии трахеи в сроке беременности 26-27 недель (рис 12).
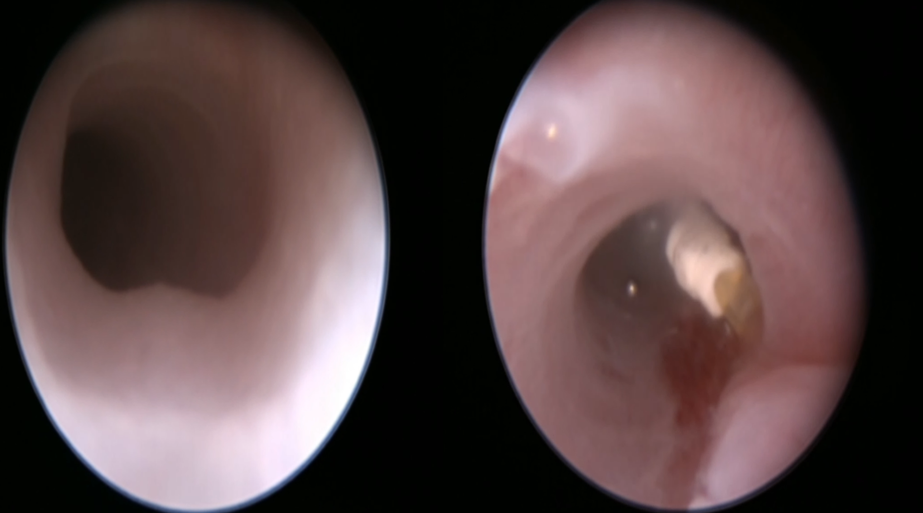
Рисунок 12. Внутриутробная трахеоскопия. «GOOLDBAL» в трахеи плода.
В 3-х случаях беременность удалось пролонгировать до 36 - 38 недель. Новорожденным проведена оперативная коррекция порока, дети выжили, растут и развиваются по возрасту. В 3 случаях в срок 31 - 32 недели произошло преждевременное излитие вод, пациентки были родоразрешены операцией кесарево сечение. Новорожденные погибли на вторые сутки жизни от дыхательной недостаточности. Эффективность баллонной окклюзии трахеи составила 50%. В институте разработана бальная оценка степени летальной гипоплазии легких у плода на основании данных УЗИ и МРТ для формирования показаний к внутриутробным вмешательствам.
7. Операции при неиммунной водянке плода. Пренатальная диагностика неиммунной водянки плода (НИВП) в настоящее время затруднений не вызывает. Основная проблема заключается в установлении причины ее развития, выборе метода лечения. Это зачастую возможно лишь в больших перинатальных центрах с хорошей лабораторной базой. Не всегда диагноз неиммунной водянки фатален.
Спектр нарушений, которые являются причиной неиммунной водянки плода, достаточно велик и примерно в 30 – 60% причины НИВП остаются неизвестными. В ФГБУ «НИИ ОММ» за период 2012-2020 гг. проведено лечение более 20 пациенток, у плодов которых диагностировали НИВП и ультразвуковые признаки анемии (рис. 6): пиковая скорость (Vp) в средне-мозговой артерии более 1,5 МоМ (G. Mari et al 1991 г.) и кардио-феморальный индекс более 0,59.
Все пациентки в первой половине II триместра беременности в 15-17 недель перенесли заболевание ОРВИ с клиническими признаками и подъемом температуры до субфебрильных цифр. Данные ультразвуковых исследований, результаты лабораторных тестов при кордоцентезах и время развития симптомов НИВП схожи. Стоит отметить что, всем плодам проведен кордоцентез с целью исключения хромосомной патологии.
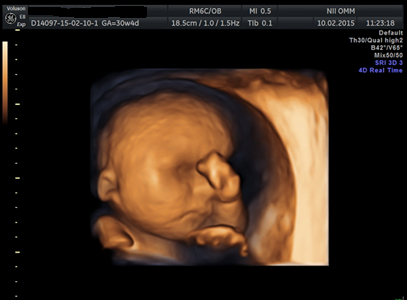 Рисунок 13. Неиммунная водянка плода в 22 недели беременности, выраженный подкожный отек у плода.
Рисунок 13. Неиммунная водянка плода в 22 недели беременности, выраженный подкожный отек у плода.
У плодов была подтверждена вирусная этиология анемии – выявлены Ig M к parvovirus B19. [19]. Поэтому беременной, перенесшей ОРВИ, необходимо регулярно (1 раз в 2 недели) проводить ультразвуковое исследование, чтобы не пропустить анемию и развитие отека плода, при котором следует решить вопрос о ранней внутриутробной внутрисосудистой гемотрансфузии и по возможности лабораторными методами типировать возбудителя.
Во всех случаях пренатального лечения НИВП анемия плода была скомпенсирована внутриутробными внутрисосудистыми переливаниями эритроцитарной массы и альбумина. Уровень Ht у плодов до операции внутриутробного переливания крови колебался от 5 до 12%. При дальнейшем динамическом ультразвуковом исследовании проявления НИВП полностью исчезли. Роды, послеродовое наблюдение женщин и обследование новорожденных проводилось в ФГБУ «НИИ ОММ». Гестационный возраст наблюдаемых детей составил 38-39 недель. Все роды были оперативными, плановая операция кесарева сечения проводилась по совокупным показаниям со стороны матери и плода. Дети растут и развиваются по возрасту.
8. Операции на сердце плода. Коллектив института имеет собственный опыт дилатации закрытого овального окна плода в 30 недель беременности у пациентки П., 36 лет, которая наблюдалась в ФГБУ «Уральский НИИ ОММ» в связи с развитием беременности на фоне сахарного диабета I типа с 20 лет. В 20 недель беременности пациентке было проведено экспертное ультразвуковое исследование и установлен диагноз: фиброэластоз эндокарда левого желудочка, критический стеноз аортального клапана, дилятационная форма с уменьшенной систолической функцией, недостаточность митрального клапана и ретроградный поток крови в восходящей аорте (рис. 14). От прерывания беременности пациентка отказалась. В сроке 27-28 недель беременности сформировалась гипоплазия левых отделов сердца (ГЛОС) с рестриктивным овальным окном. После проведения перинатального консилиума пациентке была предложена вальвулопластика овального окна.
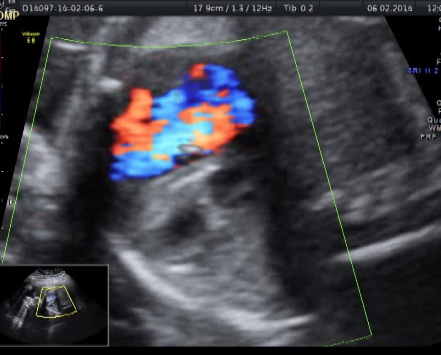
Рисунок 14. Пациентка П. 27-28 недель беременности : ГЛОС с рестрективным овальным окном
В 30 недель беременности нами совместно с сосудистым хирургом под постоянным ультразвуковым контролем проведена внутриутробная вальвулопластика овального окна. Через правое предсердие введен проводник в полость левого предсердия, затем стандартный коронарный дилятационный баллонный катетер «MINI TREK» 2,0 х 12 мм, производитель AbbotVascular, США. Баллон катетера трижды был максимально расширен, затем игла с баллонным катетером были удалены из предсердий. Во время операции особенностей в сердечной деятельности у плода зарегистрировано не было. При проведении эхокардиографии плода после операции зарегистрировано открытое овальное окно (рис.15).
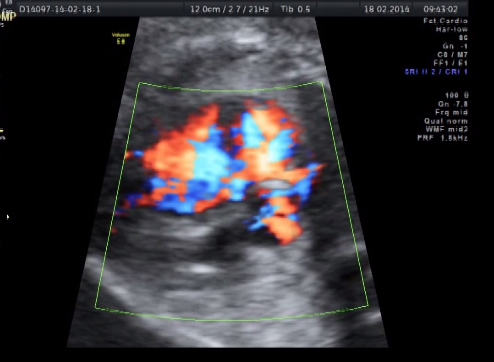
Рисунок 15. Открытое овальное окно
Пациентка П. была родоразрешена по акушерским показаниям путем операции кесарева сечения в сроке 34-35 недель. Новорожденный мальчик весом 2090 г., рост 43 см, 6/7 баллов по шкале Апгар, на самостоятельном дыхании. После консультации кардиохирурга непрерывно осуществлялось введение вазопростана с целью профилактики закрытия фетальных коммуникаций [20].
Мы предполагаем продолжить исследования в области применения баллонной вальвулопластики клапанов сердца при ГЛОС, но столкнулись с проблемой позднего направления пациентов на данную манипуляцию.
Заключение
Таким образом, мы подошли к моменту в развитии медицины, когда технические возможности позволяют заглянуть за грань ранее недоступного – внутриутробную жизнь, увидеть проблемы, с которыми плод сталкивается в своем развитии и вовремя скорректировать ситуацию. В этом нам помогает современное оборудование: ультразвуковые экспертные аппараты, МРТ, эндоскопическая техника. На сегодняшний день мы имеем возможность не только внедрять новые виды операций, но и разрабатывать собственный отечественный инструментарий.
Спинно-мозговая грыжа. Малоинвазивная фетоскопическая коррекция
Критерии отбора пациентов для проведения данного вмешательства:
- возраст 18 лет и более;
- менингоцеле, миеломенингоцеле T1 –S1;
- синдром Арнольда – Киари II типа;
- отсутствие других пороков развития;
- нормальный кариотип у плода.
Противопоказаниями для проведения операции являлись:
- отказ пациентки от операции;
- кесарево сечение в анамнезе;
- истмико-цервикальная недостаточность (цервикальный канал 2 см и менее);
- сахарный диабет I и II типа;
- гепатиты и ВИЧ инфекция;
- декомпенсированная соматическая патология;
- маловодие;
- ультразвуковые признаки внутриматочной инфекции;
- отслойка плаценты;
- предлежание плаценты;
- психические заболевания у беременной;
- плацента занимает всю переднюю стенку матки.
Методика проведения клинического этапа включала:
- УЗИ и магнитно-резонансной томография для оценки порока плода;
- интраоперационный ультразвуковой мониторинг;
- допплерографический контроль фето-плацентарного кровообращения;
- анестезиологическое обеспечение беременной женщины (эндотрахеальный наркоз) и обезболивание плода;
- обеспечение достаточного интраамниального рабочего пространства;
- эндоскопия.
Пациентам проведится полное клинико-лабораторное и инструментальное обследование. По данным УЗИ и МРТ подтверждается диагноз. (рисунок 16)
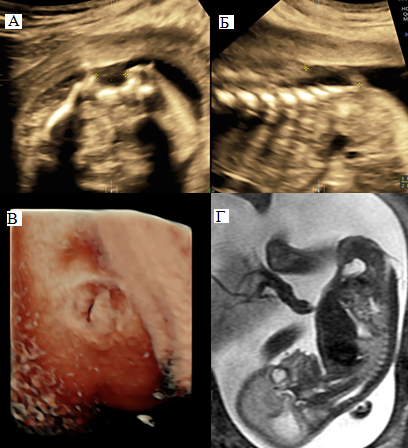
Рисунок 16. – А, Б, В – ультразвуковое исследование в 18-19 нед. Беременности –спинномозговая грыжа; Г – МРТ - исследование в 23-24 нед. беременности.
Проведится кариотипирование плода.
Пациенты информируются о наличии врожденного порока развития центральной нервной системы у плода, о благоприятном для жизни и неблагоприятном для здоровья ребенка прогнозе, методах коррекции, возможных осложнениях.
18 февраля 2020 года в ФГБУ «НИИ ОММ» Минздрава России мультидисциплинарная команда врачей Урала и Сибири успешно осуществила первую в России внутриутробную фетоскопическуюоперацию по коррекции spina bifida в сроке 27 нед. беременности.
Операционная бригада включала 11 человек: врачи акушеры – гинекологи (г. Екатеринбург, НИИ ОММ) - Косовцова Н.В., Полянин Д.В., Айтов А.Э.; детские хирурги - Козлов Ю.А., Распутин А.А (г. Иркутск, Ивано-Матренинская больница); детский нейрохирург - Ковальков К.А.(г. Кемерово, ОДКБ); анестезиологи (г. Екатеринбург, НИИ ОММ) - Кинжалова С.В., Макаров Р.А.; медсестра-анестезист (г. Екатеринбург, НИИ ОММ) - Китаева Л.В.; операционные сестры (г. Екатеринбург, НИИ ОММ) - Вишневская И.А. и Мухаметдинова Э.А.
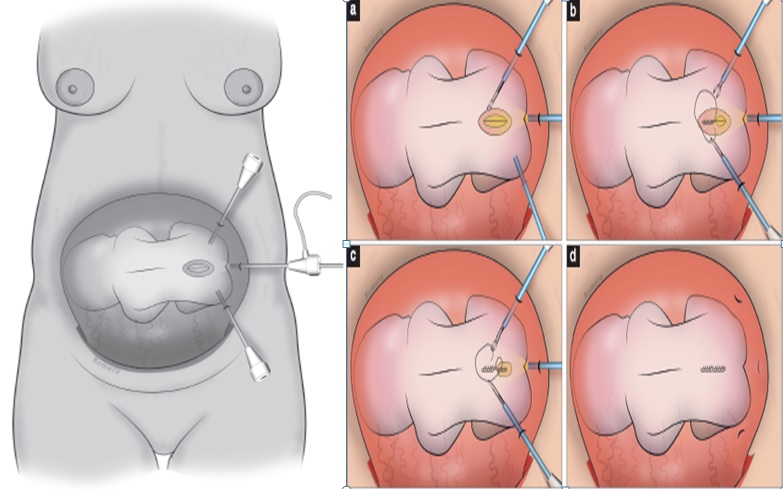
Рисунок 17 - Процедура фетоскопического двухслойного закрытия дефекта нервной трубки: (а) рассечение плакоды и резекция кисты; (б) сшивание миофасциального слоя; (в) сшивание кожи; (d) внешний вид после окончания операции.
Продолжительность оперативного вмешательства составила 4 часа 25 минут, на протяжении всей операции осуществлялся токолиз атозибаном (трактоцил) по традиционной схеме.
Этапы операции (рисунки 18-19):
I этап операции: с целью миорелаксации и обезболивания плода в вену пуповины вводились: пипекурония бромид (ардуан) 0,1 мг и фентанил 10 мкг/кг веса плода (каждый час операции).
Анестезиологическое пособие беременной – эндотрахеальный наркоз на основе газового анестетика севофлурана.
II этап операции: Матка была экстериоризирована с использованием нижне-срединной лапаротомии. Плод с помощью мягких и деликатных внешних манипуляций размещался в удобной позиции для хирурга. Используя ультразвуковое наведения, были размещены швы, фиксирующие амниотическую мембрану, чтобы сблизить ее со стенкой матки и предупредить преждевременную отслойку оклоплодного пузыря. С использованием техники Сельдингера между швами устанавливался порт размером Fr12 (COOK Inc., USA). для оптического телескопа диаметром 3.9 мм. Затем под визуальным контролем телескопа производилось наложение фиксирующих амниотическую мембрану швов в местах введения двух оставшихся портов Fr 10 (COOK Inc., USA), предназначенных для введения в полость матки сменных рабочих инструментов диаметром 3 мм - деликатных зажимов Kelly и duckbill, микроножниц Metzenbaum, крючка-коагулятора, канюли-аспиратора и иглодержателя. (рисунок 5)
III этап операции: визуализация плода. В пояснично-крестцовом отделе позвоночника определяется спинномозговая грыжа размером 20 х 15 мм, в центре имеется плакода (placode). Произведено ее диссекция из оболочек менингоцеле по краю кожно-эпителиальной зоны и свободное размещение на дне спинномозгового канала. Принимая во внимание большой диастаз между краями дефекта позвоночника, миофасциальная пластика грыжевых ворот не выполнялась. Для закрытия дефекта спинномозгового канала использовалась заплата «Durepair» (Medtronic, California, USA). Заплата фиксирована отдельными швами PDS II 6/0 r краям апоневроза. Следующим этапом проведена сепарация кожных лоскутов вокруг дефекта. В заключении произведено наложение непрерывного кожного шва над заплатой с использованием самофиксирующейся нити и системы закрытия раны V-Lok 3/0 (Medtronic, California, USA). (рисунок 6)
IV этап операции: Проведено послойное восстановление целости передней брюшной стенки.
Рисунок 18. Акушеры-гинекологи осуществляют фетоскопический доступ к спинке внутриутробного плода.
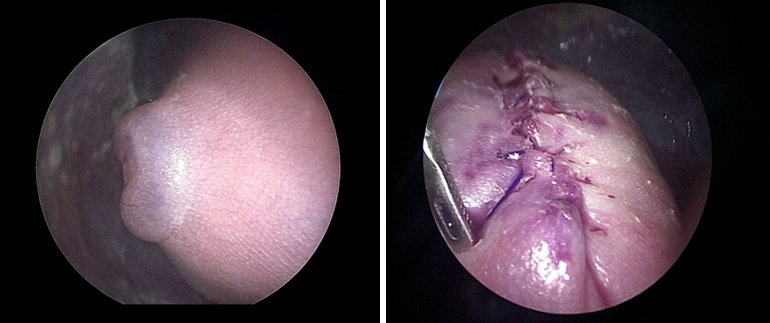
Рисунок 19 - Спинномозговая грыжа плода. Фетоскопический доступ. Внутриутробная коррекция менингомиелоцеле.
В послеоперационном периоде пациентке проводилась сохраняющая (обеспечение функционального покоя матки), антибактериальная терапия, ультразвуковое и МРТ – исследование, выписана домой на 14 сутки в удовлетворительном состоянии, под наблюдение участкового гинеколога (рисунок 20).
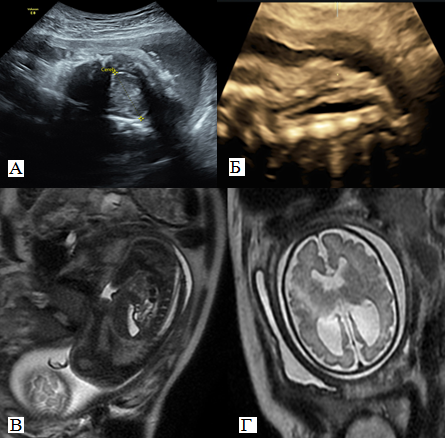
Рисунок 20 – УЗИ (после операции): А – нормальная визуализация мозжечка; Б – визуализируется шов в пояснично-крестцовом отделе позвоночника; МРТ (после операции): В - четко виден закрытый дефект спинно-мозгового канала; Г - умеренная вентрикуломегалия.
В 36 нед беременности у пациентки произошел преждевременный разрыв плодного пузыря, проведено оперативное родоразрешение путем Кесарева сечения вОПЦ г. Челябинска. Вес новорожденной девочки 2200,0 г, рост 45 см. Оценка по Апгар 8/9 баллов.
Состояние ребенка после рождения стабильное, самочувствие удовлетворительное, движения нижних конечностей не ограничено, недержание кала и мочи не наблюдается (рисунок 21).
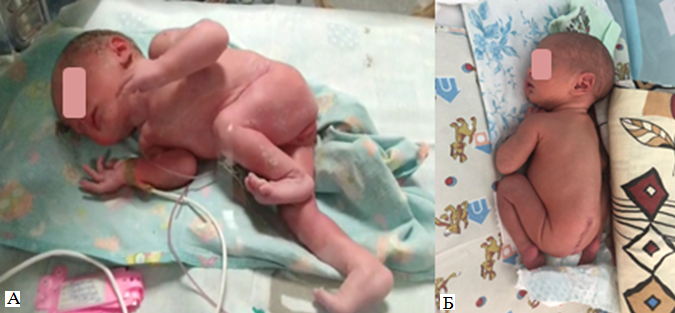
Рисунок 21 - А - движения нижних конечностей не ограничено, Б - послеоперационный рубец.
Таким образом, фетоскопическое двухслойное закрытие спинно-мозгового дефекта обеспечивает хорошее качество закрытия дефекта. Этот метод представляет вариант внутриутробного лечения spina bifida.
Фетоскопическая коррекция спинномозговой грыжи направлена на защиту ткани спинного мозга, в конечном счете, уменьшает потребность в послеродовом вентрикулоперитонеальном шунтировании и снижает процент инвалидизации детей. Фетоскопический минимальный доступ значительно снижает риск материнской травмы (нет гистеротомии).При применении ультразвукового контроля открытый фетоскопический доступ с применением трех троакаров достигается практически во всех случаях. Создание мультидисциплинарного подхода к внутриутробной коррекции spina bifida является единственно правильным решением и залогом успеха.
ИСТОЧНИКИ
- Westerburg B, Feldstein VA, Sandberg PL, Lopoo JB, Harrison MR, Albanese CT. Sonographic prognostic factors in fetuses with sacrococcygeal teratoma. J Pediatr Surg. 2000 Feb;35(2):322-5; discussion 325-6.
- Nguyen HT, Herndon CD, Cooper C, Gatti J, Kirsch A, Kokorowski P, et al. The Society for Fetal Urology consensus statement on the evaluation and management of antenatal hydronephrosis. J Pediatr Urol.2010; 6 :212–31.
- Медведев М.В. Пренатальная эхография. Пренатальный диагноз и прогноз. М.: Реал. Там. 2009. - С. 272-305.
- Wu S, Johnson MP. Fetal lower urinary tract obstruction. Clin Perinatol. 2009 Jun; 36(2):377-390.
- Coplen DE, Austin PF, Yan Y, Blanco VM, Dicke JM. The magnitude of fetal renal pelvic dilatation can identify obstructive postnatal hydronephrosis, and direct postnatal evaluation and management. J Urol. 2006;176 :724–7.
- Косовцова Н.В. Новый взгляд на лечение обструктивных уропатий у плода /Н.В. Косовцова, Н.В. Башмакова, М.В. Павличенко, Т.В. Маркова. Вопросы гинекологии, акушерства и перинатологии. – 2015. – Т. 14, №3. – С. 33-38.
- Quintero R.A., Morales W.J., Allen M.N. et al. Staging of twin-twin transfusion syndrome . J.Perinatol.1999;19: 550-555.
- Med Sci. Twin-twin transfusion syndrome. 2009 June; 24(3): 513–516. Published online 2009 June 16.
- Adedayo L, Adegbite, Styard B. Uordи, R.Bajoria J Perinat Med. Twin-twin transfusion syndrome. 2003; 23: 498-503.
- Saade G, Moise K, Forman K, et al. A randomized trial of septostomy versus amnioreduction in the treatment of twin oligohydramnios polyhydramnios sequence (TOPS) Am J Obstet Gynecol(Society for Maternal-Fetal Medicine. Oral presentation abstract 3) 2003;187.
- Parilla BV, Strasburger JF, Socol ML. Fetal supraventricular tachycardia complicated by hydrops fetalis: a role for direct fetal intramuscular therapy. Am J Perinatol. 1996; 13 :483–486.
- Косовцова Н.В., Башмакова Н.В., Маркова Т.В., Потапов Н.Н. Селективный фетоцид при осложненном течении монохориальной двойни и дихориальной тройни с использованием лазерной коагуляции сосудов пуповины. - Российский вестник акушера – гинеколога – 2016. - Т16, №1 с 45-50.
- Косовцова Н.В., Башмакова Н.В., Ковалев В.В., Маркова Т.В., Потапов Н.Н. Опыт инвазивной коррекции фето-фетального трансфузионного синдрома // Акушерство и гинекология. – 2013, №8. – С 48-54.
- Башмакова Н.В., Косовцова Н.В., Цывьян П.Б. Монохориальная двойня. Преодоление проблем в диагностике и лечении. - «Седьмой легион», 2014.
- Nicolaides KH1, Soothill PW, Rodeck CH, Clewell W.Rh disease: intravascular fetal blood transfusion by cordocentesis. Fetal Ther. 1986;1(4):185-92.
- Harrison MR, et al: A randomized trial of fetal endoscopic tracheal occlusion for severe fetal congenital diaphragmatic hernia. N Engl J Med 2003;349:1916–1924.
- Ruano R, Duarte SA, Pimenta EJ, Takashi E, da Silva MM, Tannuri U, Zugaib M. Comparison between fetal endoscopic tracheal occlusion using a 1.0-mm fetoscope and prenatal expectant management in severe congenital diaphragmatic hernia. Fetal Diagn Ther 2011; 29: 64–70.
- Deprest JA, Hyett JA, Flake AW, Nicolaides K, Gratacos E. Current controversies in prenatal diagnosis 4: should fetal surgery be done in all cases of severe diaphragmatic hernia? Prenat Diagn. 2009;29(1):15-19.
- Dreux S, Salomon LJ, Rosenblatt J, Favre R, Houfflin-Debarge V, Broussin B, Guimiot F, Fenaux H, Delezoide AL, Muller F Biochemical analysis of ascites fluid as an aid to etiological diagnosis: a series of 100 cases of nonimmune fetal ascites. Prenat Diagn. 2015;35(3):214.
- Косовцова Н.В., Башмакова Н.В., Маркова Т.В., Потапов Н.Н. Вариант внутриутробной коррекции осложнения гипопластического синдрома левых отделов сердца. - Российский вестник акушера-гинеколога – 2015. – Т. 14, №1, с. 56-59.